전세계 휩쓴 'GLP-1 계열' 신약 개발 H.O.P 프로젝트 가동오너가 장녀가 지휘···'에페글레나타이드' 국내 임상3상 중'HM15136'와 병용요법 전임상 단계, MASH 신약도 속도

한미약품이 차세대 글로벌 블록버스의 의약품으로 떠오르고 있는 비만·MASH(대사이상 관련 지방간염) 치료제 개발에 집중하며 제2의 도약에 도전하고 있다.
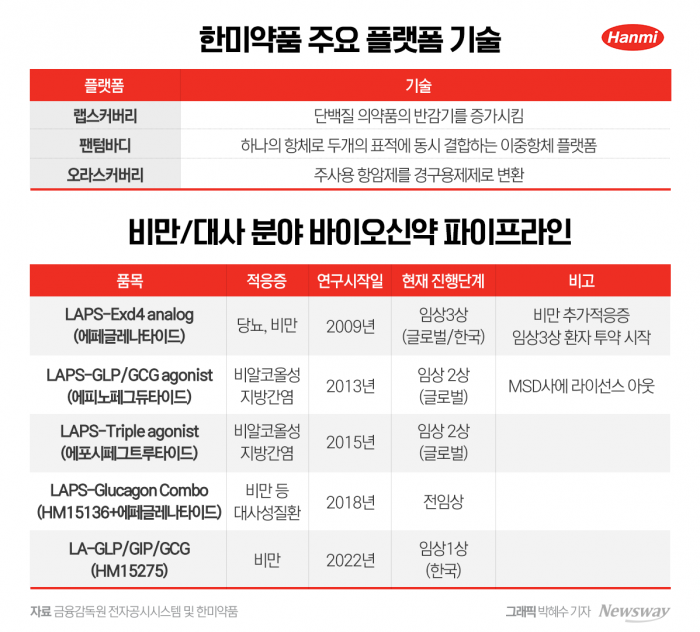
19일 관련 업계에 따르면, 한미약품은 오너가 장녀 임주현 한미사이언스 전략기획실장(한미약품 사장)의 지휘 아래 비만 프로젝트인 'H.O.P(Hanmi Obesity Pipeline)'를 가동하고 글루카곤 유사 펩타이드(GLP)-1 계열 신약 개발에 집중하고 있다.
GLP-1 계열은 주로 당뇨 치료제로 사용되던 물질로, 체내에서 인슐린 분비를 유도해 혈당 수치를 조절하는 GLP-1 호르몬의 유사체로 작용한다. 췌장의 베타 세포에서 생성되는 이 호르몬은 체내 인슐린 합성 및 분비, 혈당량 감소, 위장관 운동 조절, 식욕 억제 등에 관여하는 것으로 알려진다.
특히 기존 식욕억제제들처럼 뇌에 명령을 내려 식욕을 억제하는데도 항정신성의약품과 같은 의존 문제 위험이 크지 않아 비만 치료 패러다임의 변화를 이끌고 있다. 뛰어난 체중감량 효과로 전세계에서 판매량이 급증하고 있는 '위고비'(성분명 세마글루티드) , '삭센다'(성분명 리라글루티드), '젭바운드'(성분명 터제파타이드) 등도 같은 계열이다.
GLP-1 제제가 비만약으로 쓰이면서 글로벌 비만치료제 시장은 급속도로 커지고 있다. 미국 투자은행(IB) 골드만삭스는 글로벌 비만치료제 시장이 2023년 60억달러(약 8조원)에서 2030년 1000억달러(약 134조원)으로 커질 것으로 보고 있다.
한미약품이 개발 중인 GLP-1 계열 파이프라인 중 임상 진행이 가장 빠른 물질은 '에페글레나타이드'다.
'에페글레나타이드'는 한미약품이 지난 2009년부터 연구개발을 시작한 물질이다. 2015년 글로벌 제약기업 사노피에 기술이전했으나 2020년 6월 계약 권리가 반환되며 한미약품이 후속 개발을 통해 비만 등 대사질환 분야에서 새로운 가능성을 모색해왔다.
회사는 자사 독자 플랫폼 기술 '랩스커버리'를 적용해 일주일에 한 번 투여하는 주사 제형의 대사질환 치료제로 '에페글레나타이드'를 개발해오다가 비만치료제로 적응증을 변경하기 위해 지난해 8월 국내 식품의약품안전처에 임상 3상 시험계획(IND)을 제출했고, 10월 승인 후 2개월여 만에 첫 환자 등록을 마쳤다.
'랩스커버리'는 지난 2022년 미국 식품의약국(FDA)의 문턱을 넘은 한미약품의 바이오신약 '롤베돈(미국 제품명, 한국 제품명: 롤론티스)'에 적용되며 상용화 가능성을 입증한 바 있다. 이 기술은 단백질 의약품의 반감기를 늘려주는 혁신적 플랫폼이다. 단백질 의약품의 경우 인체에 투여됐을 때 반감기가 짧아 자주 투여를 해야 하는 불편함이 있는데, 랩스커버리는 투여 횟수 감소로 환자의 삶의 질을 높이고, 투여량을 감소시킴으로써 부작용을 줄이는 한편 효능을 개선한다.
현재 한미약품은 '에페글레나타이드'를 국내 시장에 우선 출시하는 것을 목표로 한국인 비만 기준(체질량지수 25kg/㎡, 대한비만학회)에 최적화된 비만 신약으로 개발 중이다. 글로벌 제약사들의 GLP-1 계열 약물들은 상대적으로 BMI 수치가 높은 서양인 환자들을 타깃으로 개발됐으나 한미약품은 한국인 체형과 체중을 반영하겠다는 계획이다.
한미약품은 GLP-1와 함께 위 억제 펩타이드(GIP), 글루카곤(GCG) 등 각각의 수용체 작용을 최적화해 비만 치료에 특화한 차세대 삼중작용제 'HM15275'도 개발 중이다.
GIP는 GLP-1 수용체 작용제의 약리학적 이점을 향상시키는 한편 메스꺼움과 구토, 설사 등 일반적인 위장관 부작용을 완화할 수 있다. GCG는 포만감 조절과 함께 에너지 소비 및 지질 대사 조절에 관여한다.
회사는 최근 식약처에 최근 건강한 성인 및 비만 환자를 대상으로 'HM15275'의 안전성과 내약성, 약동학, 약력학 특성 등을 평가하는 임상1상 시험계획(IND)을 제출했으며, 이달 중 FDA에도 IND를 제출한다는 계획이다.
'HM15275'는 한미의 기존 바이오신약 플랫폼 '랩스커버리'가 아닌 '아실레이션(Acylation) ' 기술이 적용됐다. 한미약품은 GLP-1/GIP/GCG 세 가지 약리작용을 적절히 활용하면 비만뿐만 아니라 제2형 당뇨병 및 심혈관 질환에 대한 치료 잠재력도 극대화할 수 있을 것으로 보고 있다.
앞선 비임상 연구에서 HM15275는 근 손실은 최소화하면서도 수술적 요법에 따른 체중감량 효과에 버금가는 효능은 물론, 다양한 대사질환 모델에서 기존 비만치료제 대비 우수한 치료 효능을 입증했다.
이와 함께 회사는 '에페글레나타이드'와 선천성 고인슐린증 치료제로 개발 중인 'HM15136'의 병용요법(LAPS-Glucagon 콤보)으로 비만 등 대사성질환 타깃 치료제를 개발 중이다. LAPS-Glucagon 콤보는 현재 전임상 단계다.
'HM15136'은 비임상 연구에서 지질 프로파일, 신장 기능 및 혈압 개선과 함께 현저한 체중 감소 효과가 관찰된 바 있다. 선천성 고인슐린증 치료제로는 임상 2상 단계에 있어 안전성이 입증된 상태다.
'HM15136'의 경우 지난 2020년 동반 질환이 있는 비만 또는 과체중 환자 대상으로도 국내 및 미국 임상 1상을 진행한 바 있다.
한미약품은 최근 새롭게 열리고 있는 MASH 분야 치료제 개발에도 속도를 내고 있다.
MASH는 기존 NASH(비알코올성지방간염)이라는 명칭을 사용했으나 미국 간질환연구협회 등 해외학회에서 명칭 변경을 결의하면서 MASH로 불리고 있다. 이 질환은 알코올 섭취와 관계없이 간세포에 중성지방이 축적되는 질환으로, 간경화, 간암, 간부전 등 심각한 간질환을 일으킬 수 있다. 전 세계적으로 유병률은 2~4%, 미국의 경우는 3~5%에 달하지만 신약개발이 어려운 분야여서 마땅한 치료제는 상태였다.
데이터 분석기업 글로벌데이터에 따르면, MASH 치료 시장 규모는 2029년 272억 달러(약 36조원)까지 성장할 것으로 전망된다.
다만 얼마 전 세계 최초의 MASH 치료제가 탄생함에 따라 이를 이을 차기 후보물질에 대한 관심이 높아지고 있는 상황이다. 앞서 FDA는 지난 14일(현지시간) 마드리갈 파마슈티컬스 MASH 치료제 '레즈디프라'(성분명 '레스메티롬')의 사용을 승인했다. 레즈디프라는 하루 한 번씩 복용하도록 설계된 경구용 치료제로, 세계 최초의 MASH 치료제다.
한미약품은 GLP-1 계열의 MASH 치료제 '에피노페그듀타이드'와 '에포시페그트루타이드'를 개발 중이다.
당초 비만 당뇨 치료제로 개발되던 '에피노페그듀타이드'는 지난 2019년 글로벌 제약사 얀센으로부터 기술반환된 후 적응증을 MASH 분야로 변경하고 2020년 미국 MSD에 재수출했다. 현재 미국 MSD가 글로벌 2b상을 순조롭게 진행하고 있다.
에피노페그듀타이드는 GLP-1 수용체와 에너지 대사량을 증가시키는 GCG 수용체를 동시에 활성화하는 이중 작용제다.
같은 적응증으로 개발한 '에포시페그트루타이드' 역시 글로벌 임상 2상에 진입하며 임상 개발에 더욱 속도를 내고 있다. '에포시페그트루타이드'는 GCG/GIP/GLP 삼중 작용 유도체다.
이밖에도 회사는 GLP-1 제제 사용시 나타날 수 있는 근육량 손실을 방지해 체중 감량의 퀄리티를 개선하고 요요 현상 억제에도 도움을 줄 수 있는 바이오신약과, 폭식 등 섭식장애를 개선할 수 있는 후보물질도 최근 도출하는 등 활발한 연구개발을 진행 중이다.
아울러 현재 경구용 펩타이드 플랫폼 기술 개발에도 착수해 상용화 가능성을 확인했으며, 최대한 빠른 시일 내에 먹는 형태의 GLP-1 제제 개발에도 나선다는 계획이다.
한미약품은 임 사장의 리더십을 기반으로 H.O.P 프로젝트를 한미의 차세대 핵심 성장동력으로 삼아 전사적 노력을 쏟겠다는 방침이다. 그 일환으로 회사는 R&D 비용도 과감하게 늘리고 있다.
회사는 지난해 R&D 비용으로 매출 대비 13.8%인 2050억원을 투입했다. 지난 2021년엔 1615억원을, 2022년엔 1779억원을 R&D에 투입했다.
연구인력도 2022년 584명에서 지난해 637명으로 1년새 53명 늘렸다. 이 중 박사급은 78명으로 전년 74명보다 4명 늘었고, 석사급은 297명으로 전년 277명 대비 20명 늘었다.
회사 측은 "'R&D는 한미의 핵심 가치'라는 경영 철학에 따라 신약 연구개발에 다시 박차를 가하고 있다"고 전했다.

뉴스웨이 유수인 기자
suin@newsway.co.kr
저작권자 © 온라인 경제미디어 뉴스웨이 · 무단 전재 및 재배포 금지









댓글